Die Peritonealdialyse (PD) ist eine patientenzentrierte Therapie. Es hat sich gezeigt, dass patientenorientierte Ansätze die Patienten aktiv einbeziehen, ihr Wohlbefinden steigern, die Versorgungsqualität verbessern und die Nachhaltigkeit des Gesundheitssystems erhöhen.1 Weltweit wurden 2020 rund 413.000 Patienten mit terminaler Niereninsuffizienz mit Peritonealdialyse (PD) behandelt, Tendenz steigend.2
Neben der Anwendung zu Hause bietet die PD weitere Vorteile für Patienten:
- Bessere Erhaltung der Nierenrestfunktion als bei HD3,4
- Kein Gefäßzugang erforderlich (z. B. Fistel)3,4
- Mit der Heimdialyse werden Patienten unabhängiger und flexibler bei der Planung
- Weniger Zeitaufwand für die Anreise und Aufenthalte in Dialyseeinrichtungen5,6
- Die Dialyse kann besser in den Alltag integriert werden und kann eine verbesserte Reisefähigkeit ermöglichen6
- Die PD hat die gleiche Überlebensrate wie die konventionelle HD. Patienten mit neu diagnostiziertem Nierenversagen können davon profitieren, wenn sie innerhalb der ersten Jahre der Dialyse eine Peritonealdialyse durchführen.6,7
CAPD: Individuelle klinische Lösungen zur Anpassung der Therapie an Ihre Patienten
Im Bereich der kontinuierlichen ambulanten Peritonealdialyse (continuous ambulatory peritoneal dialysis, CAPD) sind unsere individuellen klinischen Lösungen auf die Anpassung der Therapie speziell für Ihre Patienten ausgelegt. Das CAPD-Behandlungssystem stay•safe enthält die Sicherheitsfunktionen DISC und PIN, welche direkt mit den PD-Lösungen verbunden sind. Das stay•safe System – kleine Details, die einen großen Unterschied machen.

Die Technologien der PIN und stay•safe DISC wurden entwickelt, um die Schulung der Patienten zu erleichtern und die Behandlung angenehmer zu gestalten

mit der stay•safe DISC, die Patienten durch die Dialyse führt

mit einem einzigartigen PIN, der die Katheterverlängerung vor der Diskonnektion verschließt8

Die geführte Behandlung erhöht die Patienten-Compliance und reduziert Fehler in der Anwendung.

Der stay•safe Organizer vereint alle Systemkomponenten, die Ihre Patienten für die Behandlung benötigen

Patienten können die Vorzüge einer CAPD-Therapie mit stay•safe auch unterwegs in vielen Ländern genießen

Verpflichtung zu mehr Nachhaltigkeit durch „PVC-freie“ und weichmacherfreie Systemkomponenten (Flüssigkeitsbeutel, Drainagebeutel und Schläuche) aus Materialien wie Biofine

Verschiedene Produkte von Fresenius Medical Care zum Einmalgebrauch bei der Peritonealdialyse wurden mit dem Nordischen Umweltzeichen zertifiziert
APD: individuelle und mit der Zeit anpassbare Behandlung
So individuell wie Ihre Patienten: sleep•safe harmony
Wie kann ein einziger Cycler speziell auf die Bedürfnisse Ihrer Patienten zugeschnittene Therapieoptionen bieten?
In einer kleinen Studie zur Benutzerfreundlichkeit von Reitz et al. zeigte der sleep•safe harmony Cycler eine gute Erlernbarkeit und Anwenderfreundlichkeit.9
In der adaptierten APD-Therapie (aAPD) mit sleep•safe harmony können Sie Sequenzen von kurzen Verweilzeiten und kleinen Füllvolumina mit langen Verweilzeiten und großen Füllvolumina und unterschiedlichen Glukosekonzentrationen kombinieren. Diese von Fischbach et al. vorgeschlagene Art der PD-Verschreibung hat das Potenzial, die Ultrafiltration (UF) und die Clearance innerhalb einer PD-Sitzung zu verbessern.10
sleep•safe harmony bietet:
- Personalisierte Behandlung nach den Bedürfnissen Ihrer Patienten. Flexible Behandlungsoptionen mit integrierter FlexPoint Technologie
- Adaptierte APD-Therapieoption, die nachweislich die Ultrafiltration und Clearance verbessert10,11
- Integrierte Bildschirmanimationen zur Anleitung und erleichterten Einrichtung12
- Verschreibung am Cycler und über die PatientOnLine-Software zur Unterstützung des Therapiemanagements (muss separat erworben werden)
Vielfältiges Schulungsangebot für die PD
Erste Schritte mit CAPD
Wir unterstützen Sie mit einer Reihe spezifischer Schulungen als Grundlage für einen gelungenen Therapiestart. Und während sich die Teilnehmer auf die Therapie vorbereiten, helfen wir dabei, in den vier Wänden Ihrer Patienten alles zum Laufen zu bringen.
Schulen
Unterstützung durch klar strukturierte Schulungen für Pflegekräfte und Patienten
Start
- Ein Expertenteam hilft Ihnen bei der Einrichtung des Systems für den Heimgebrauch
- Starter-Kit mit Informationen für medizinisches Fachpersonal (Healthcare Professionals, HCPs) zur Einrichtung einer häuslichen Therapieeinheit

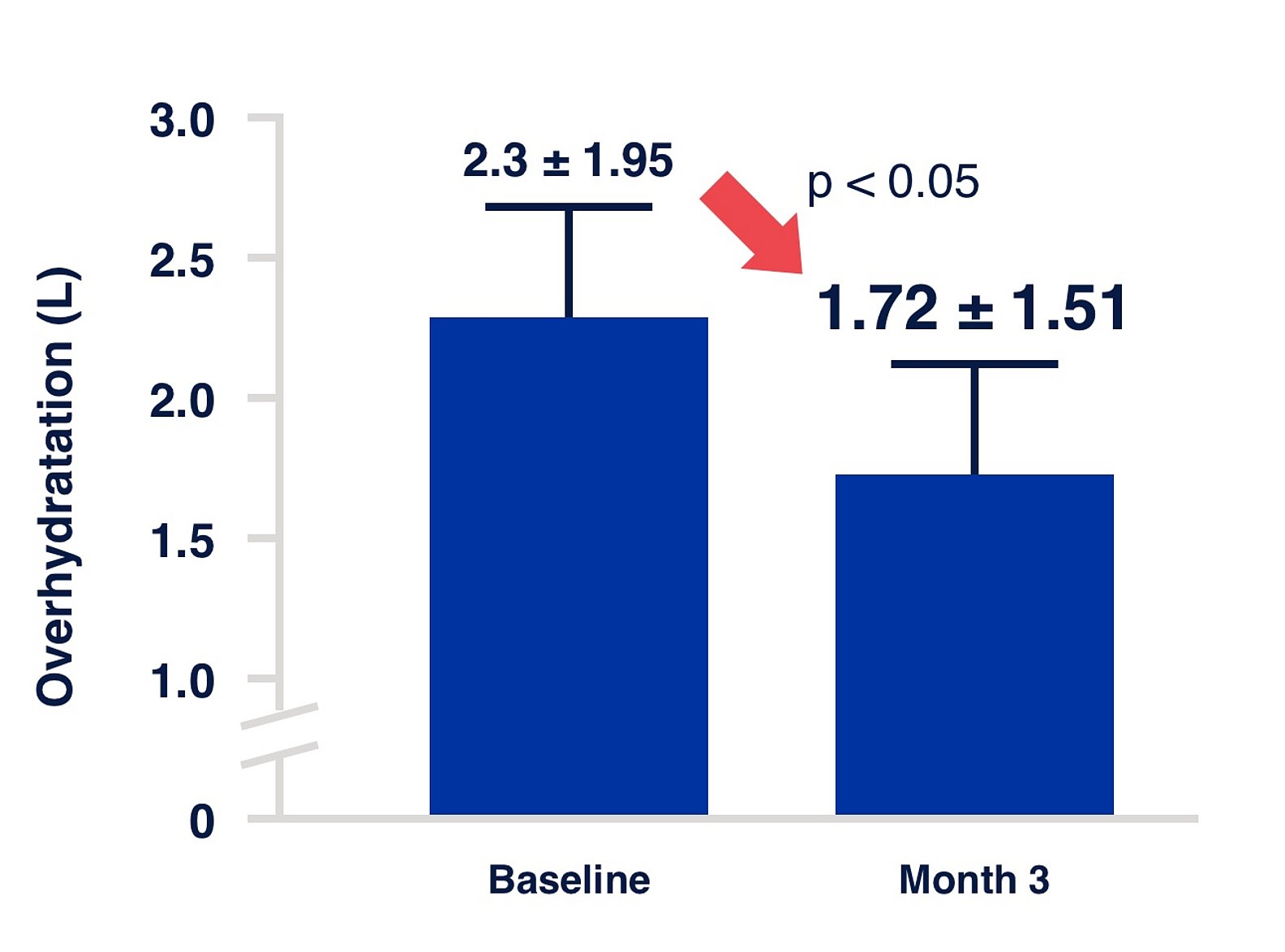
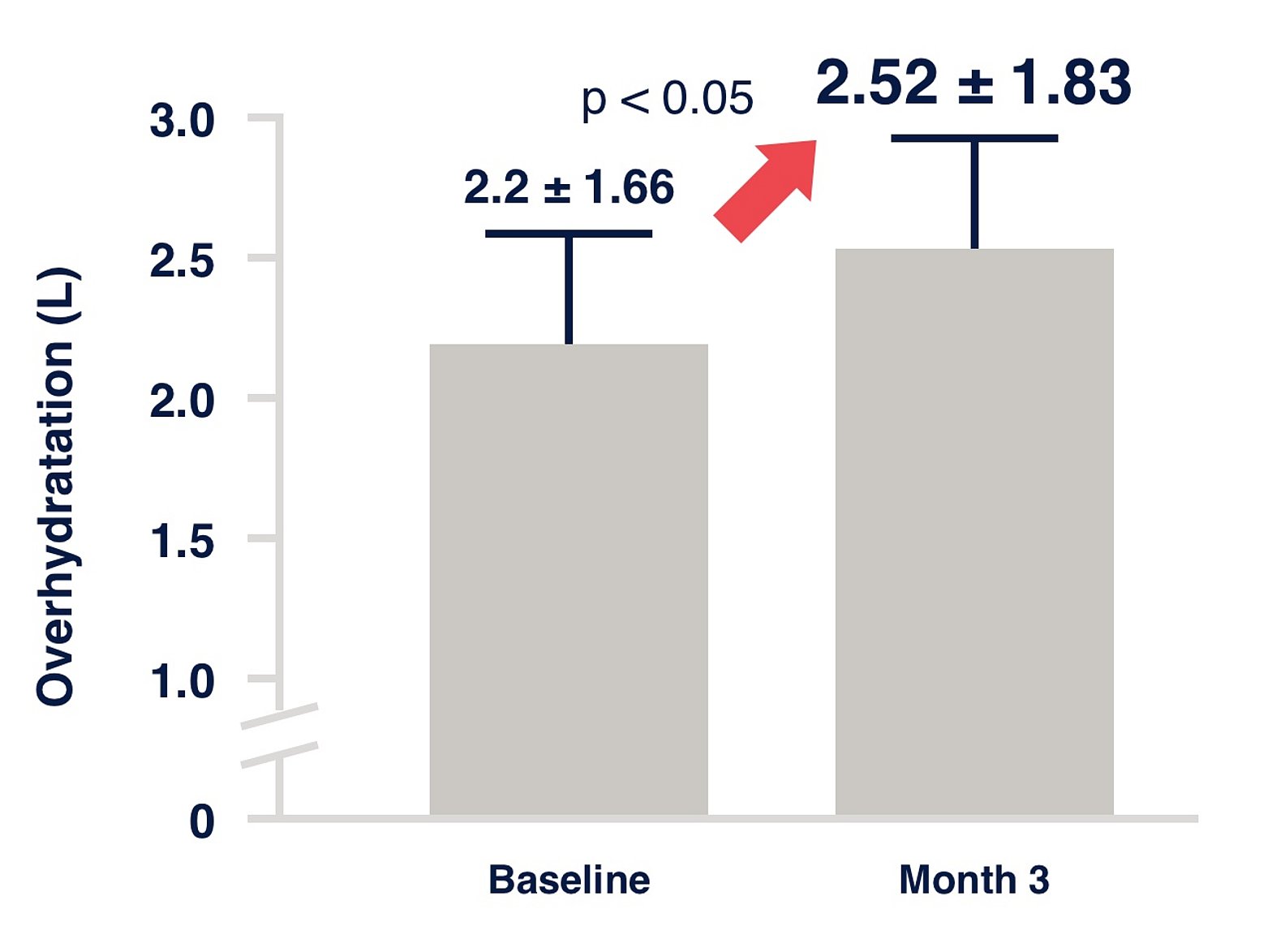
Abbildung 1:
Studieninformationen
Flüssigkeitshaushalt bei Beginn der PD. Prospektive Kohortenstudie in 135 Prüfzentren in 28 Ländern.17 Die IPOD-PD-Studie hat gezeigt, dass eine Flüssigkeitsüberladung bereits zu Beginn der PD hochprävalent ist.18
Individualisierung der PD mit Flüssigkeitsmanagement
Eines der größten Probleme in der heutigen Nierenersatztherapie ist die quantitative Beurteilung und Steuerung des Flüssigkeitshaushalts. Es gibt viele Faktoren, die bekanntermaßen den Flüssigkeitshaushalt beeinträchtigen, wie Komorbiditäten, Medikation, Ernährung und Behandlungsmodalitäten.13,14
Die Behandlung eines Flüssigkeitsungleichgewichts bei Dialysepatienten ist aufgrund seiner Rolle bei der Entwicklung von Herz-Kreislauf-Erkrankungen wichtig, die die Haupttodesursache bei Dialysepatienten darstellen.15 Die Herstellung einer Euvolämie ist daher ein Hauptziel der PD, da sowohl Dehydrierung als auch Hyperhydratation die Mortalität durch das kardiovaskuläre Risiko und die Beeinträchtigung der Nierenrestfunktion (Residual Kidney Function, RKF) erhöhen können.14,16
Wichtige Faktoren für den Flüssigkeitshaushalt sind:
- Die UF allein kann bei der Beurteilung des Flüssigkeitshaushalts von Patienten irreführend sein.
- Um das Flüssigkeitsvolumen des Patienten zu verbessern, sollte sowohl die Zufuhr als auch die Abgabe kontrolliert werden.
- Der Blutdruck kann ein irreführender Parameter zur Beurteilung des Flüssigkeitshaushalts sein und zu falschen Therapieentscheidungen führen.
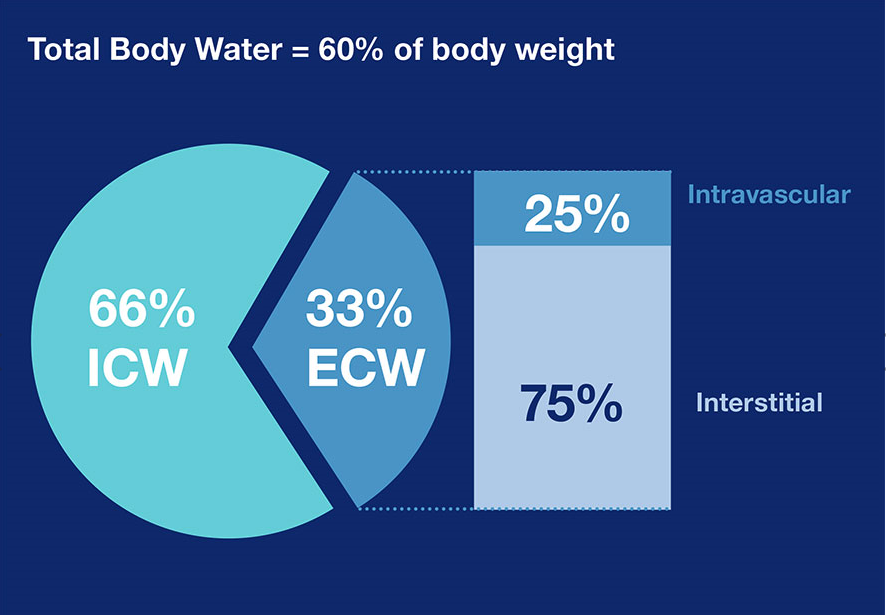
Abbildung 2: Verteilung des TBW21
ISPD-Leitlinien/-Empfehlungen – Richtlinie zu Zielen für die Ableitung von gelösten Substanzen und Flüssigkeit bei erwachsenen Patienten mit chronischer Peritonealdialyse
Die ISPD-Leitlinien legen nahe, dass die klinische Beurteilung ein vielfältiges Spektrum klinischer Parameter und Laborergebnisse umfassen sollte, einschließlich peritonealer und renaler Clearance, Hydratationsstatus, Appetit- und Ernährungszustand, Energieniveau, Hämoglobinkonzentration, Ansprechen auf Erythropoetin-Therapie, Elektrolyte und Säure-Basen-Gleichgewicht, Calciumphosphat-Homöostase sowie Blutdruckkontrolle (Evidenzgrad C).19
Eine Flüssigkeitsüberladung wird durch die Expansion des extrazellulären Wassers ausgelöst. Bei der Untersuchung einer Flüssigkeitsüberladung ist es wichtig, das Gesamtkörperwasser (TBW) in intrazelluläres (ICW) und extrazelluläres Wasser (ECW) zu unterteilen. Letzteres ist weiter untergliedert in zirkulierende und interstitielle Kompartimente.20,21
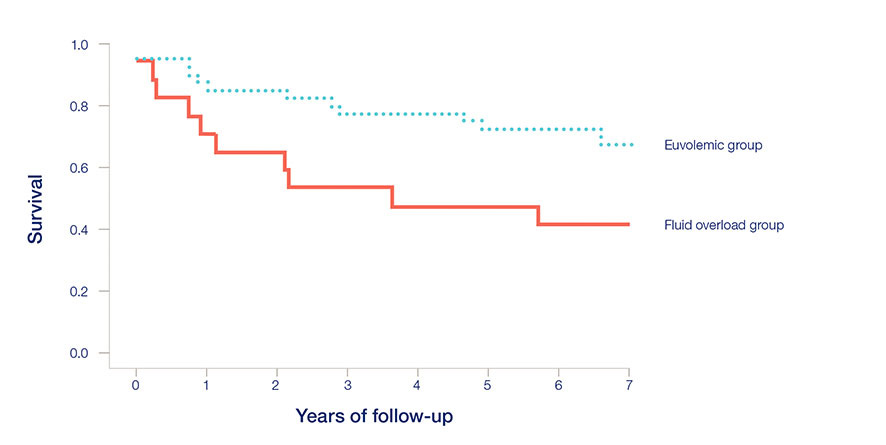
Abbildung 3:
Überlebenskurven bei euvolämischen und flüssigkeitsüberladenen Patienten16
Studieninformationen
Monozentrische, observatorische Querschnittstudie, mit bis zu 6,5 Jahren Nachverfolgung
Hydratation gemessen mit dem Body Composition Monitor (BCM)
Ein Schritt-für-Schritt-Ansatz
Für Patienten mit Peritonealdialyse (PD) potenziell lebensbedrohlich: Flüssigkeitsüberladung
Das Flüssigkeitsmanagement ist bei Patienten mit Peritonealdialyse (PD) äußerst wichtig, denn es gilt als gesichert, dass:
- flüssigkeitsüberladene PD-Patienten ein signifikant höheres Mortalitätsrisiko haben als euvolämische Patienten.16
Volumenkontrolle – drei Schritte für eine bessere Volumenkontrolle
Dieser Schritt-für-Schritt-Ansatz wurde entwickelt, um Ihre PD-Patienten zu unterstützen. Basierend auf unserer Erfahrung und unserem breit gefächerten Portfolio bieten wir Lösungen für jeden Schritt des Flüssigkeitsmanagements. Unsere Produkte und Dienstleistungen decken den gesamten Prozess ab und bieten die Möglichkeit, die Behandlungsergebnisse zu verbessern.

Experten der International Society for Peritoneal Dialysis (ISPD) empfehlen die regelmäßige klinische Beurteilung des Flüssigkeitshaushalts.19
Der Body Composition Monitor (BCM) ist eine Ergänzung zur Routineuntersuchung Ihrer Patienten und wird in vielen PD-Zentren aktiv eingesetzt. Er unterstützt die Entscheidungsfindung im therapeutischen Management der Volumenkontrolle bei PD-Patienten. Bei jedem Kontrolltermin können Sie den tatsächlichen Flüssigkeitshaushalt Ihrer Patienten beurteilen und überwachen, sodass Sie Probleme frühzeitig erkennen und gegebenenfalls korrigierend eingreifen können.22
Wir empfehlen die klinische Überprüfung des Hydratationsstatus regelmäßig bei jeder Nachuntersuchung bzw. bei klinischer Indikation häufiger.23
| Dehydratation | Normalhydratation | Hyperhydratation |
|---|---|---|
| Hypotonie | Normotonie | Hypertonie |
| Verlust der RKF | Erhaltung der RKF/Reduzierung des kardiovaskulären Risikos | Verlust der RKF/LVH |
| Erhöhte Mortalität | Höhere Überlebensrate | Erhöhte Mortalität |
Gründe für bessere Aufnahmekontrolle
Eine übermäßige Zufuhr von Natrium aus der Nahrung ist für PD-Patienten schnell gesundheitsschädigend. Sie erhöht die extrazelluläre Osmolarität und führt zu
- Verlagerung von Wasser aus dem intrazellulären in das extrazelluläre Kompartiment und damit zu einer Ausdehnung des Volumens25
- Stimulierung des Durstgefühls26
Trotz der Bedeutung dieses Themas zeigte eine systematische Prüfung der einschlägig anerkannten Fachliteratur zur Einhaltung von Ernährungsrichtlinien, dass bis zu 67 % der Patienten diese nicht befolgen.27
Daher müssen weitere Anstrengungen unternommen werden, um die Einhaltung der Grenzwerte von PD-Patienten für die Aufnahme von Salz und Flüssigkeit zu verbessern. Jede Verbesserung der Aufnahmewerte erleichtert die Korrektur des Flüssigkeitsungleichgewichts.
Längerer Erhalt der Nierenrestfunktion (Residual Kidney Function, RKF) und Anwendung des adaptierten PD-Verschreibungskonzepts
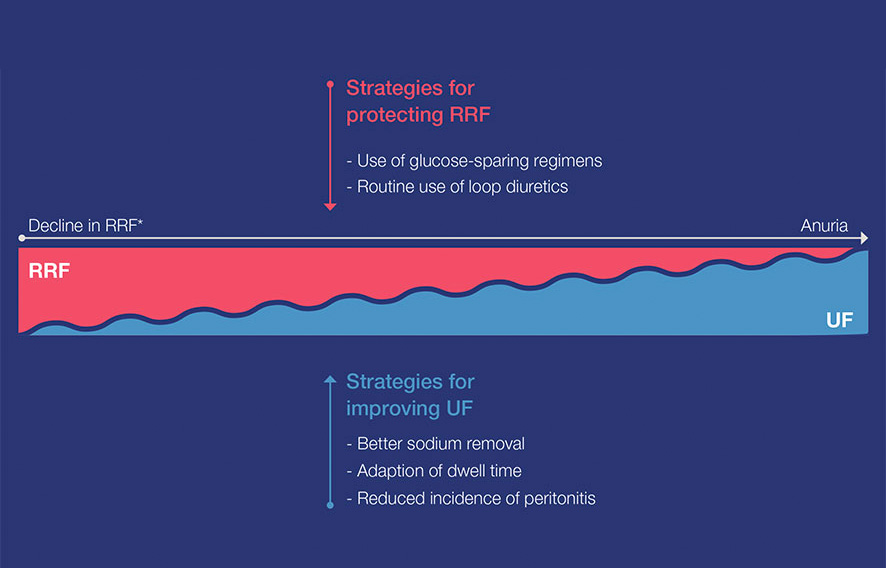
Abbildung 6: Die Abbildung zeigt die Abnahme der Nierenrestfunktion (Residual Kidney Function, RKF; fiktive Darstellung)
* Vorgeschlagenes Modell der Beziehung zwischen RKF und UF: vereinfachte Darstellung der natürlichen Abnahme der Nierenfunktion. Diese Abnahme kann bei einzelnen Patienten sehr unterschiedlich ausfallen.
Verbesserung der Flüssigkeitsausscheidung bei PD-Patienten
Die Leistung der Niere
Der Rückgang der RKF wirkt sich auf die klinischen Ergebnisse aus. Der Verlust der RKF löst nicht nur eine Flüssigkeitsüberladung aus, sondern trägt auch zu Entzündungen, Anämie, Mangelernährung, LVH, Hypertonie und Herz-Kreislauf-Erkrankungen bei.28
Der Beitrag der Technik
Mit der Abnahme der RKF bei chronischem Nierenversagen wird die Ultrafiltration (UF) über PD wichtiger und schwieriger. Die PD ermöglicht eine individuelle Dialyse-Verschreibung durch die Kombination verschiedener Techniken, Dialyselösungen sowie einer variierenden Anzahl und Dauer der Verweilphasen.17
Angesichts der Bedeutung der RKF und UF für ein erfolgreiches Flüssigkeitsmanagement sind klinische Strategien zur RKF-Erhaltung und -Verbesserung von überragender Bedeutung.
Erhaltung der RKF und UF-Kapazität für verlängerte Flüssigkeitsausscheidung
Die RKF ist relevant für die Entfernung von Flüssigkeiten und gelösten Substanzen. Die Aufrechterhaltung der RKF ist wichtig für die Urinproduktion und die Regulierung des Flüssigkeitshaushalts. Die Verwendung von PD-Lösungen leistet daher einen wichtigen Beitrag zum Flüssigkeitsmanagement Ihres Patienten.29
Gemäß den Richtlinien wird die Verwendung von PD-Lösungen empfohlen, die dazu beitragen, die schädlichen Auswirkungen einer chronischen Exposition der Peritonealmembran zu reduzieren und die Membranfunktion länger zu erhalten.30,31,32
Wichtige Faktoren für den Flüssigkeitshaushalt sind:
- Die UF allein kann bei der Beurteilung des Flüssigkeitshaushalts von Patienten irreführend sein.
- Der Flüssigkeitshaushalt ist hauptsächlich das Ergebnis des Gleichgewichts zwischen Aufnahme und Ausscheidung über die Zeit. Um den Flüssigkeitshaushalt eines Patienten zu verbessern, sollten beide Seiten kontrolliert werden, um etwaige Tendenzen zu bestimmen13
- Der Blutdruck kann zur Beurteilung des Flüssigkeitshaushalts irreführend sein und zu falschen Therapieentscheidungen führen13
1 Europäische Kommission, Mitteilung der Kommission an das Europäische Parlament, den Rat, den Europäischen Wirtschafts- und Sozialausschuss und den Ausschuss der Regionen über die Ermöglichung der digitalen Umgestaltung der Gesundheitsversorgung und Pflege im digitalen Binnenmarkt 2018
2 Fresenius Medical Care, Geschäftsbericht 2020
3 Chan CT et al. Am J Kidney Dis 2019; 73(3):363-371
4 Auguste BL et al. Can J Kidney Health Dis 2019
5 Suri RS et al. Kidney Int. 2015; 88(2):360-8
6 Argilés A et al. Nephrology Dialysis Transplantation 2020; 35(11):1863-1839
7 Kumar VA et al. Kidney Int 2014; 86(5):1016-1022
8 Fresenius Medical Care, www.freseniusmedicalcare.asia/en/healthcare-professionals/home-therapies/staysafe-and-biofine/; 03/2022
9 Reitz T et al. Renal Replacement Therapy 2021; 7(20)
10 Fischbach M et al. Perit Dial Int 2011; 31(4):450-458
11 Vera M et al. PLoS One 2021; 16(12)
12 Punzalan S et al. Journal of Kidney Care 2017; 2(5):262-267
13 Ronco C et al. Contrib Nephrol 2012;178:164-168
14 Yong-Lim K et al. Seminars in Nephrol 2017; 37(1):43-53
15 Shu Y et al. Blood Purif 2018; 46(4):350-358
16 Jotterand Drepper V et al. PLoS One 2016; 11(7):e0158741
17 Van Biesen W et al. Clin J Am Soc Nephrol 2019; 14(6): 882-893
18 Ronco C et al. Nephrol Dial Transplant 2015; 30(5):849-858
19 Lo Wk et al. Perit Dial Int 2006; 26(5):520-522
20 Kim YL et al. Semin Nephrol 2017; 37(1):43-53
21 Chan et al. Eur J Comp Anim Pract 2014; 24:14-23
22 Cader RA et al. J Clin Nurs 2013; 22:741-748
23 Wang AY et al. Perit Dialysis Int 2015; 35:379-387
24 Luo YJ et al. Blood Purif 2011; 31:296-302
25 Wilson J et al. Semin Dial 2014; 17(4):260-4
26 Ahmad S et al. Semin Dial 2004; 17(4):284-7
27 Griva K et al. PLoS One 2014; 25;9(2):e8900
28 Marron B et al. Kidney Int Suppl 2008; 108:42-51
29 Xin L et al. Center for Kidney Diseases Nanjing Medical University 2016
30 Williams JD et al. Kidney Int 2004; 66(1):408-18
31 Weiss L et al. Perit Dial Int 2009; 29(6):630-633
32 Rippe B et al. Kidney Int 2001; 59(1):348-57